
来自柏林夏里特医学院,马克斯普朗克分子遗传学研究所(MPIMG)和石勒苏益格-荷尔斯泰因大学医院(UKSH)的研究人员详细研究了BPTA综合征(一种
来自柏林夏里特医学院,马克斯普朗克分子遗传学研究所(MPIMG)和石勒苏益格-荷尔斯泰因大学医院(UKSH)的研究人员详细研究了BPTA综合征(一种极其罕见的遗传性疾病)是如何产生的。蛋白质电荷的变化会破坏细胞的自我组织,导致发育障碍。研究小组还确定了数百种与各种疾病相关的可比遗传变化,例如大脑发育障碍和癌症易感性。这种机制现在已经在《自然》杂志*上进行了描述,可能是许多无法解释的疾病和健康状况的原因。
数以千计的遗传变化与各种疾病、紊乱和病症有关。但是,这些突变究竟是如何产生疾病的,目前还很少清楚。这是因为这些变化与具有无序三维结构的蛋白质部分和细胞内的功能有关,到目前为止,人们对此知之甚少。“很难研究这些蛋白质片段负责做什么,因为在许多情况下,它们在产生效果之前必须与其他分子相互作用,”Charité医学与人类遗传学研究所的Martin Mensah博士说。他是该研究的两位第一作者之一,也是Charité与柏林卫生研究所(BIH)合作的数字临床科学家计划的研究员。“以BPTA综合征为例,我们现在已经详细描述了蛋白质无序区域的变化如何导致遗传疾病。这意味着研究小组发现了一种导致遗传性疾病的新机制 - 而且,根据这项研究,令人惊讶的是,这种机制并不那么罕见。
BPTA 代表“短指趾、多指和胫骨发育不全/发育不全”。患者有累及四肢、面部、神经系统和骨骼以及其他器官的严重畸形。全世界记录在案的病例不到十例,使这种疾病极为罕见。为了确定这种综合征的原因,研究人员解码了五名受影响患者的遗传信息,并发现所有患者的HMGB1蛋白都发生了变化。由于所谓的移码突变,蛋白质结构的最后三分之一具有正电荷,而不是通常的负电荷。
核仁凝固
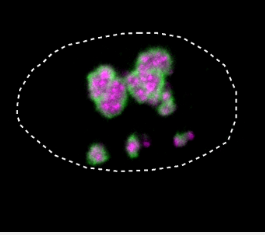
电荷的变化意味着HMGB1类似于倾向于聚集在核仁中的蛋白质,核仁是细胞核中的一小块区域,细胞蛋白质工厂的一部分组装在那里。这种作用使细胞核仁对细胞的活力至关重要。正如研究小组基于分离蛋白质和细胞培养物的实验所表明的那样,突变的HMGB1蛋白现在具有带正电荷的末端部分被不恰当地吸引到核仁。而且由于蛋白质的延伸也变得更硬,HMGB1蛋白也聚集在一起。“在显微镜下,我们能够看到这导致核仁失去其自身的液体状特性并变得越来越坚硬,”MPIMG研究员,该研究的另一位第一作者Henri Niskanen博士解释说。
核仁的这种凝固会对细胞的重要功能产生不利影响。与没有突变的细胞相比,具有突变蛋白的细胞在培养物中死亡。UKSH人类遗传学研究所所长,该研究的三位主要作者之一Malte Spielmann教授博士提供了他的结论:“我们展示了蛋白质无序部分的突变如何导致疾病。当电荷发生变化时,蛋白质错误地积聚在核仁中,对其重要功能产生不利影响。这导致生物体发育的紊乱。
对现有疾病的新解释
根据他们的初步发现,研究人员搜索了包含数千人DNA序列的数据库,寻找类似的案例。他们能够在600种蛋白质中鉴定出66多个突变,这些突变使蛋白质的最后一部分具有正电荷和更硬的特性。在这些突变中,有101个以前与各种疾病有关,包括神经发育障碍和对癌症的易感性增加。对于13种选定的蛋白质,研究小组研究了细胞培养物,以了解突变是否使它们对核仁具有特殊的亲和力。其中12个就是这种情况。大约一半的蛋白质测试损害了核仁的功能,因此它们与BPTA综合征的疾病机制相似。
“我们在BPTA综合征中发现的导致这种疾病的机制也可能与许多其他疾病和病症有关,”该研究的第一作者Denise Horn教授说,他在Charité的医学和人类遗传学研究所工作。“所以我们打开了一扇门,可以帮助解释许多其他疾病。真正的工作现在就开始了。
新发现的机制也可能导致新的治疗方法,至少对于某些疾病。“肿瘤可归因于受影响细胞的遗传变化,”MPIMG研究小组负责人,该研究的第三位主要作者Denes Hnisz博士解释说。“这意味着我们可能能够通过干预细胞的自组织来防止癌症在未来发展,这种自组织是由蛋白质的无序部分介导的。
声明本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们