
2023 年 7 月 20 日宣布,食品和药物管理局 (FDA)、犹他大学骨科创新中心 (OIC)、骨科系和 Spencer Fox Eccles 医学院宣布,一
2023 年 7 月 20 日宣布,食品和药物管理局 (FDA)、犹他大学骨科创新中心 (OIC)、骨科系和 Spencer Fox Eccles 医学院宣布,一种名为 Bone Bolt System 的新骨折固定系统已批准上市。
“这一成就表明了骨科致力于提供新的创新解决方案,以提高骨科患者护理质量,”杰克和黑泽尔·罗伯逊总统教授兼骨科系主任 Darrel S. Brodke 医学博士说。“正是我们的临床教师、实习生、我们的发现研究小组和我们的创新研究小组(称为 OIC)之间的动态合作,促成了这一进步,这是未来众多进步中的第一个。”
FDA 授予 Bone Bolt System 在销售和营销该设备的 510(k) 许可。这一里程碑标志着犹他大学历史上首次有新型医疗设备获得 FDA 510(k) 许可。
犹他大学校长泰勒·兰德尔 (Taylor Randall) 表示:“作为领先的研究型大学之一,创新在我们改善患者生活质量的使命中发挥着核心作用,OIC 的骨螺栓系统正是做到了这一点。” “该设备不仅会对我们在犹他大学健康中心提供的护理产生影响,而且表明我们致力于通过尽快将其推向市场,将研究转化为现实世界的影响,以更广泛地改善健康结果。”
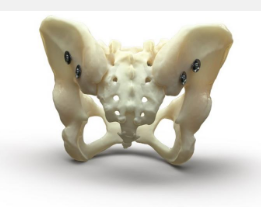
骨螺栓系统是OIC设计和开发的一种用于经皮骨折固定的新型植入系统。该系统是一整套不同长度和直径的植入物,以及相关的手术器械和灭菌托盘。这些植入物用于治疗具有挑战性的骨折,例如骨盆骨折以及手臂和腿部的长骨骨折。骨螺栓系统受专利号 11,553,948 的保护,其他和国际专利正在申请中。
OIC 向 FDA 提交了 510(k) 报告,以证明该医疗器械与现有 FDA 510(k) 批准的器械安全有效,或“基本等效”。经 FDA 510(k) 批准后,医疗器械可在合法销售
OIC 开发的骨螺栓系统完全符合 FDA 质量体系法规和 ISO 13485 医疗器械质量管理体系。此外,OIC 还为骨螺栓系统开发了一条商业供应链。下一步,由 OIC 和犹他大学 PIVOT 中心领导,将建立行业合作伙伴关系,将骨螺栓系统商业化,并将其带到全国各地的医院和手术中心,造福骨科患者。
“骨螺栓手术的简单性可有效稳定复杂骨折,这将影响具有挑战性的骨折患者的护理标准。骨螺栓系统开发过程中的深思熟虑鼓励快速采用,因为开发团队将护理人员的观点与临床结果结合起来考虑,”PIVOT 创新与商业化副总监 Huy Tran 说道。“PIVOT Center 期待与潜在的行业合作伙伴合作,将该技术商业化,并对患者的生活质量产生立竿见影的影响。”
声明本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们